-
-
藥品生產(chǎn)企業(yè)集中QA管理系統(tǒng)(CQA)
利用先進(jìn)的技術(shù),將”人,、機(jī),、料、法,、環(huán)“五個(gè)關(guān)鍵質(zhì)量要素有機(jī)結(jié)合,,確保數(shù)據(jù)準(zhǔn)確、及時(shí),、完整,、可追溯的實(shí)時(shí)監(jiān)管預(yù)警分析追溯系統(tǒng)
系 統(tǒng) 概 述
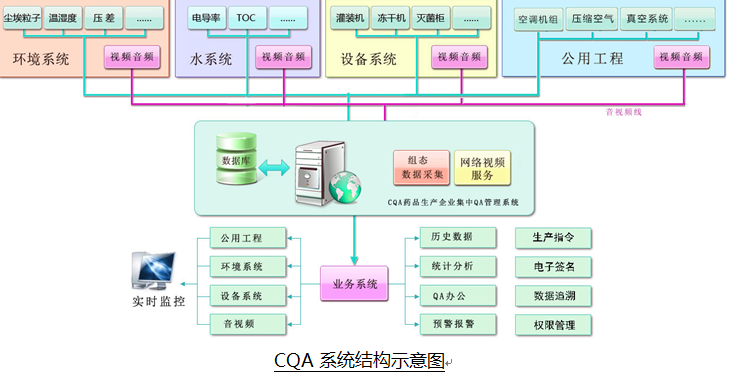
“耀智CQA藥品生產(chǎn)企業(yè)集中CQA質(zhì)量管理系統(tǒng) (以下簡(jiǎn)稱YOZEE-CQA)”為藥品生產(chǎn)企業(yè)及質(zhì)量保證人員提供全面、完整,、高效的質(zhì)量保證管理平臺(tái),,主要利用視頻監(jiān)控、音頻通信,、數(shù)據(jù)采集等技術(shù)實(shí)現(xiàn)質(zhì)量保證人員對(duì)生產(chǎn)區(qū)域中的設(shè)備運(yùn)行狀態(tài),、人員工作情況等的監(jiān)控;系統(tǒng)將QA日常工作納入管理,,實(shí)現(xiàn)規(guī)范,、完整的電子化數(shù)據(jù),實(shí)現(xiàn)質(zhì)量保證人員的信息化辦公,。
利用平臺(tái)提供的統(tǒng)計(jì)分析功能,,實(shí)現(xiàn)各生產(chǎn)批次設(shè)備、環(huán)境,、用水,、公用等系統(tǒng)的數(shù)據(jù)匯總,結(jié)合質(zhì)量保證人員填寫的記錄,,實(shí)現(xiàn)質(zhì)量保證環(huán)節(jié)的生產(chǎn)記錄功能,,并提供按生產(chǎn)批次的導(dǎo)出功能。同時(shí),系統(tǒng)提供偏差處理,、風(fēng)險(xiǎn)評(píng)估等的報(bào)告填寫及導(dǎo)出功能,。
利用電子簽名實(shí)現(xiàn)人員信息的數(shù)據(jù)身份識(shí)別,,在保證合規(guī)性的同時(shí)使人員操作(如批次信息制定、產(chǎn)品配方制定,、生產(chǎn)執(zhí)行時(shí),,應(yīng)使用雙重身份認(rèn)證,實(shí)現(xiàn)電子簽名)具有法律效力,。
提供完善的數(shù)據(jù)備份及恢復(fù)方案,,利用服務(wù)器本身的雙硬盤配置RAID1結(jié)構(gòu),實(shí)現(xiàn)服務(wù)器實(shí)時(shí)硬盤備份,,避免因硬盤壞道,、損壞等產(chǎn)生的數(shù)據(jù)丟失或無法正常存取數(shù)據(jù);利用異地備份等形式實(shí)現(xiàn)數(shù)據(jù)實(shí)時(shí)備份,,避免因服務(wù)器宕機(jī)引起的數(shù)據(jù)丟失,;集中CQA質(zhì)量管理系統(tǒng)利用數(shù)據(jù)庫自身機(jī)制實(shí)現(xiàn)數(shù)據(jù)庫快照及增量備份,便于在數(shù)據(jù)庫崩潰時(shí)快速恢復(fù)數(shù)據(jù)到最新備份點(diǎn),。
借助加密手段對(duì)數(shù)據(jù)庫訪問鏈路、應(yīng)用程序訪問,、權(quán)限控制等增加安全措施,,保證系統(tǒng)數(shù)據(jù)及訪問的安全、可靠,、一致,、準(zhǔn)確。
 |  |
系 統(tǒng) 背 景
藥品生產(chǎn)企業(yè)質(zhì)量保證人員在工作中需要全面了解生產(chǎn)活動(dòng)中的各項(xiàng)數(shù)據(jù),,如設(shè)備狀態(tài),、生產(chǎn)環(huán)境、工藝參數(shù)等的變化,;生產(chǎn)批次信息與各種數(shù)據(jù)的關(guān)聯(lián)關(guān)系,,如生產(chǎn)記錄中需要的該批次工藝參數(shù)、環(huán)境數(shù)據(jù)等,;在生產(chǎn)過程中需與生產(chǎn)人員進(jìn)行適當(dāng)交流,;將偏差處理、風(fēng)險(xiǎn)評(píng)估,、GMP認(rèn)證管理等內(nèi)容進(jìn)行信息化管理,,以便形成系統(tǒng)化管理。
2010版對(duì)數(shù)據(jù)與記錄管理的要求 第一百五十八條 良好的文件是質(zhì)量保證系統(tǒng)的基本要素,,本規(guī)范所指的文件包括質(zhì)量標(biāo)準(zhǔn),,工藝規(guī)程、操作規(guī)程,、記錄,、報(bào)告等,。…… 第一百六十五條 記錄應(yīng)留有數(shù)據(jù)填寫的足夠表格,。記錄應(yīng)及時(shí)填寫,,內(nèi)容真實(shí),字跡清晰,、易讀,,不易擦掉 第一百六十六條 應(yīng)盡可能采用生產(chǎn)和檢驗(yàn)設(shè)備自動(dòng)打印的記錄,圖譜和曲線圖等,,并表明產(chǎn)品或樣品的名稱,、批號(hào)和記錄設(shè)備的信息。操作人應(yīng)簽注姓名和日期,。 第一百六十七條 記錄應(yīng)報(bào)紙清潔,,不得撕毀和任意涂改,記錄填寫的任何更改都應(yīng)簽注姓名和日期,,并使原有信息仍清晰可辨,,必要時(shí),應(yīng)說明更改的理由,。記錄如需重新譽(yù)寫,,則原有記錄不得銷毀,而應(yīng)作為重新譽(yù)寫記錄的附件保存,。 | 2010版對(duì)數(shù)據(jù)與記錄管理的要求 第一百六十八條 與本規(guī)范有關(guān)的沒想活動(dòng)均有記錄,,所有記錄至少應(yīng)保存至藥品有效期后一年,確認(rèn)和驗(yàn)證,、穩(wěn)定性考察的記錄和報(bào)告等重要文件應(yīng)長期保存,,以保證產(chǎn)品生產(chǎn)、質(zhì)量控制和質(zhì)量保證等活動(dòng)可以追溯,。 每批藥品應(yīng)有批記錄,,包括生產(chǎn)記錄、批包裝記錄,、批檢驗(yàn)記錄和藥品放行審核記錄等與本批產(chǎn)品有關(guān)的記錄和文件,。批記錄應(yīng)由質(zhì)量管理部門負(fù)責(zé)管理。 第一百六十九條 如使用電子數(shù)據(jù)處理系統(tǒng),、照相技術(shù)或其他可靠方式記錄數(shù)據(jù)資料,,應(yīng)有所用系統(tǒng)的詳細(xì)規(guī)程;記錄的準(zhǔn)確性應(yīng)經(jīng)過核對(duì),,如果使用電子數(shù)據(jù)批記錄系統(tǒng),,只有授權(quán)人員方可通過計(jì)算機(jī)輸入或更改數(shù),更改和刪除情況應(yīng)有記錄:應(yīng)使用密碼或其它方式來限制數(shù)據(jù)系統(tǒng)的登陸:關(guān)鍵數(shù)據(jù)輸入后,,應(yīng)由他人獨(dú)立進(jìn)行復(fù)核,。用電子方法保存的批記錄,,應(yīng)采用磁帶、縮微膠卷,、紙質(zhì)副本或其他方法進(jìn)行備份,,以確保記錄的安全,且數(shù)據(jù)資料在保存期內(nèi)應(yīng)便于查閱,。 |
2010版對(duì)數(shù)據(jù)與記錄管理的要求 第二百二十一條 質(zhì)量控制實(shí)驗(yàn)室的文件應(yīng)當(dāng)符合第八章的原則,,并符合下列要求: (一) 質(zhì)量控制實(shí)驗(yàn)室應(yīng)到至少有下列詳細(xì)文件; 1、 質(zhì)量標(biāo)準(zhǔn); 2,、 取樣操作規(guī)程和記錄,; 3、 檢驗(yàn)操作規(guī)程和記錄(包括檢驗(yàn)記錄或?qū)嶒?yàn)室工作記事簿),; 4,、 檢驗(yàn)報(bào)告或證書; 5,、 必要的環(huán)境監(jiān)測(cè)操作流程,、記錄和報(bào)告; 6,、 必要的檢驗(yàn)方法驗(yàn)證報(bào)告和記錄,; 7、 儀器校準(zhǔn)和設(shè)備使用,、清潔,、維護(hù)的操作規(guī)程及記錄,; (二) 每批藥品的檢驗(yàn)記錄應(yīng)當(dāng)包括中間產(chǎn)品,、待包裝產(chǎn)品和成品的質(zhì)量檢驗(yàn)記錄,可追溯該批藥品所有相關(guān)質(zhì)量檢驗(yàn)情況,。 (三) 宜采用便于趨勢(shì)分析的方法保存某些數(shù)據(jù)(如檢驗(yàn)數(shù),、環(huán)境監(jiān)測(cè)數(shù)據(jù)、制藥用水的微生物監(jiān)測(cè)數(shù)據(jù)),。 (四) 除與批記錄相關(guān)的資料信息外,,還應(yīng)保存其他原始資料或記錄,以方便查閱,。 | 醫(yī)藥工業(yè)發(fā)展規(guī)劃指南 應(yīng)用信息技術(shù)改進(jìn)質(zhì)量管理,。建立生產(chǎn)質(zhì)量信息實(shí)時(shí)監(jiān)控系統(tǒng),實(shí)現(xiàn)質(zhì)量數(shù)據(jù)的自動(dòng)采集,、管理和可追溯,,保證數(shù)據(jù)的真實(shí)性和完整性。開發(fā)應(yīng)用基于過程分析技術(shù)的智能化控制系統(tǒng),,建立質(zhì)量偏差智能預(yù)警系統(tǒng),,最大限度約束,、規(guī)范和減少員工操作,促進(jìn)GMP嚴(yán)格執(zhí)行,,有效保證產(chǎn)品質(zhì)量穩(wěn)定,。 |
系統(tǒng)建設(shè)目標(biāo)
以數(shù)據(jù)采集、視頻監(jiān)控,、音頻通迅等手段為基礎(chǔ),,結(jié)合質(zhì)量保證人員工作中的側(cè)重點(diǎn),形成一套數(shù)據(jù)完整,、可靠,、高效的集中質(zhì)量保證平臺(tái);通過利用數(shù)據(jù)的自動(dòng)采集,、預(yù)警報(bào)警,、統(tǒng)計(jì)匯總減少因人為因素造成的數(shù)據(jù)偏差;通過增加音視頻通訊手段減少質(zhì)量保證人員進(jìn)出潔凈區(qū)的次數(shù),,減少因人為因素造成的安全隱患,;通過將生產(chǎn)批次與數(shù)據(jù)采集相結(jié)合,實(shí)現(xiàn)批次化生產(chǎn)工藝數(shù)據(jù)的完整性管理,并提供按生產(chǎn)批次數(shù)據(jù)包的導(dǎo)出功能,。集中CQA質(zhì)量管理系統(tǒng)的建設(shè)需要符合計(jì)算機(jī)化系統(tǒng)驗(yàn)證要求,,遵循GMP、 21 CFR PART 11等相關(guān)法規(guī),。
數(shù)據(jù)安全,、準(zhǔn)確、一致,、可驗(yàn)證,、可追溯是項(xiàng)目建設(shè)的基本目標(biāo)。
系 統(tǒng) 功 能
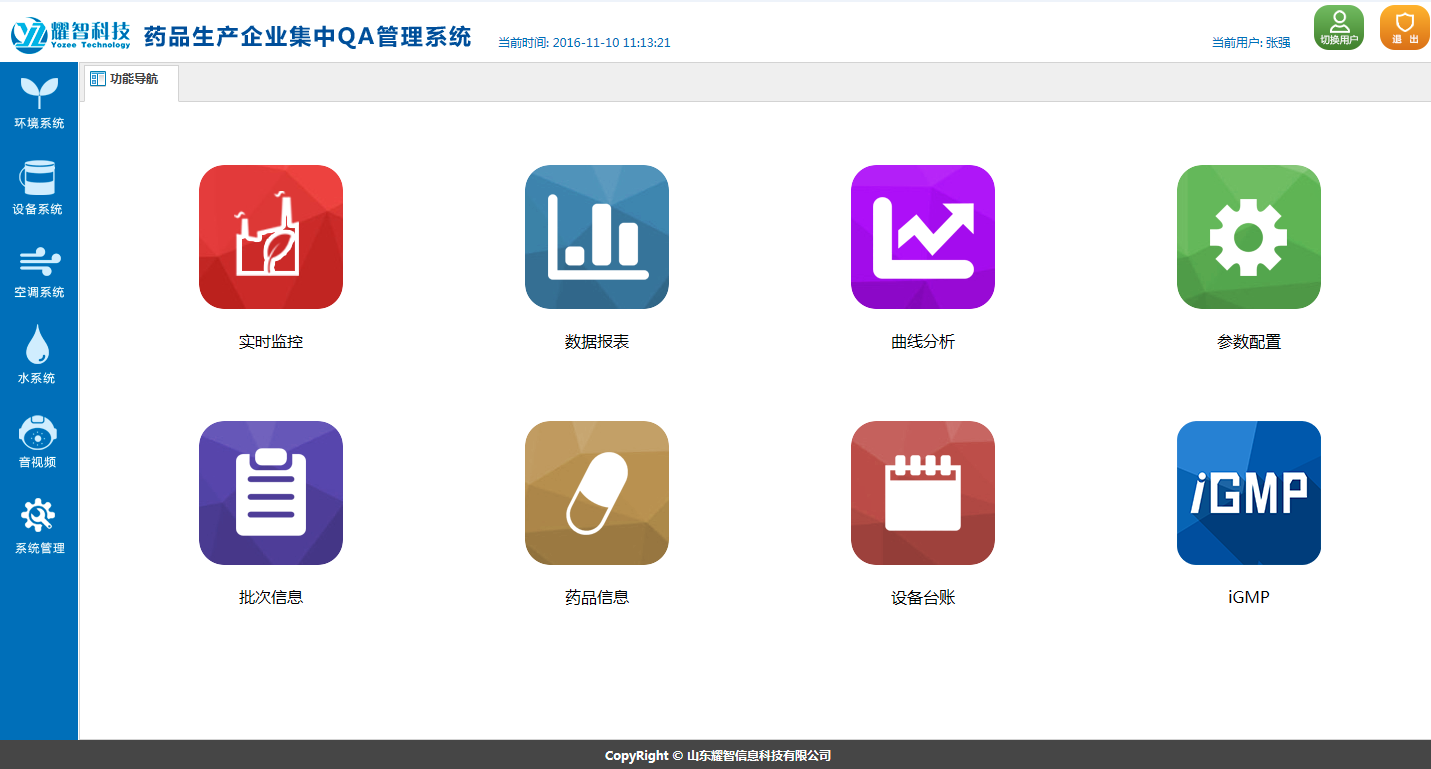 | 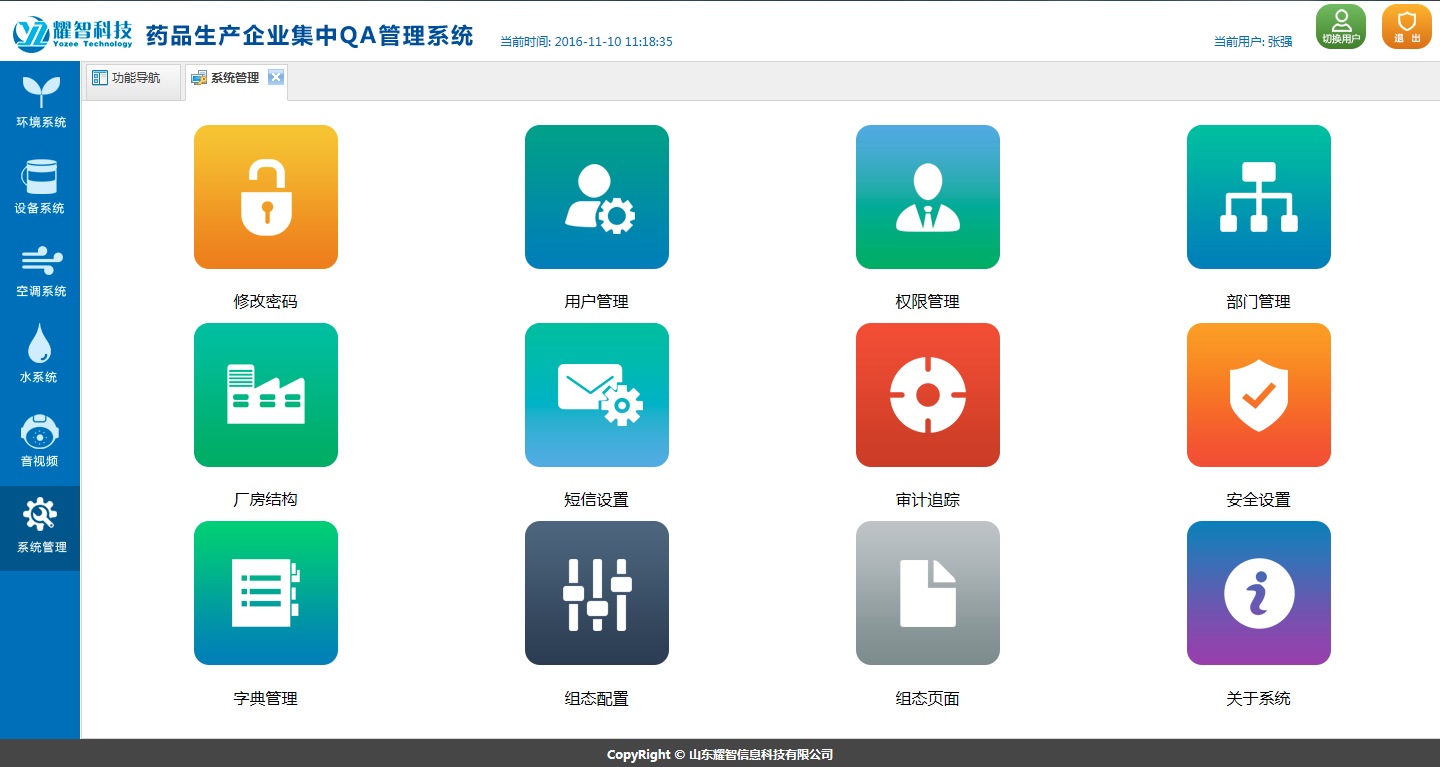 |
以上資料來自山東耀智信息科技有限公司官方網(wǎng)站,,網(wǎng)址:http://rnvmpl.com.cn



